A. 184,1 gam và 91,8 gam.
B. 84,9 gam và 91,8 gam.
C. 184,1 gam và 177,9 gam.
D. 84,9 gam và 86,1 gam.
Hòa tan hỗn hợp X gồm 0,2 mol Fe3O4; 0,25 mol Fe và 0,25 mol Cu vào dung dịch HCl 1M
và HNO3 3M thu được dung dịch Y (chỉ chứa muối Fe(II) và Cu(II)) và khí NO là sản phẩm khử duy
nhất. Cho Y tác dụng với dung dịch AgNO3 dư thu được kết tủa Z. Khối lượng muối trong dung dịch
Y và khối lượng của Z lần lượt là
A. 184,1 gam và 91,8 gam. B. 84,9 gam và 91,8 gam.
C. 184,1 gam và 177,9 gam. D. 84, 9 gam và 86,1 gam.
đáp số: C
Hòa tan vừa hết hỗn hợp Q gồm 0,3 mol Fe3O4, 0,25 mol Fe và 0,2 mol CuO vào dung dịch hỗn hợp HCl 3M và HNO3 4M. Sau phản ứng hoàn toàn thu được dung dịch Y (chỉ chứa Fe3+ và Cu2+ và khí NO (là sản phẩm khử duy nhất). Tổng khối lượng muối trong dung dịch là
A. 268,2 gam
B. 368,1 gam
C. 423,2 gam
D. 266,9 gam
Đây là 1 bài tập tổng hợp khá khó, đòi hỏi phải tính toán khá nhiều song hướng giải lại rất cụ thể và rõ ràng đó là ta sẽ sử dụng định luật bảo toàn khối lượng để tính khối lượng muối:
![]()
Do đó nhiệm vụ bây giờ là phải tìm được
![]()
+) Tính được khối lượng hỗn hợp Q dễ dàng:
![]()
+) Vì HCl và HNO3 trong cùng 1 dung dịch cho nên tỉ lệ về số mol cũng chính là tỉ lệ về nồng độ.
Gọi n H C l = 3 a t h ì n H N O 3 = 4 a
⇒maxit = 3a.36,5 + 4a.63 = 361,5a (gam)
+) Sơ đồ bài toán:
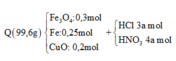
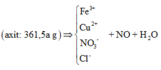
+) Ta lần lượt đi tìm các yếu tố còn thiếu:
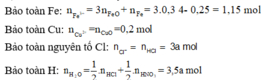
+) Áp dụng định luật bảo toàn điện tích ta có:
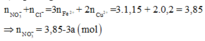
Tiếp tục sử dụng bảo toàn N:
![]()
![]()
Ta có:
m m u ố i = m F e 3 + + m C u 2 + + m C l - + m N O 3 -
![]()
= 315,9 - 79,5a (g)
Bây giờ ta cần phải tìm được a, nên nhớ là ta đã có các biểu diễn các yếu tố cần tìm theo a, do đó ta sử dụng định luật bảo toàn khối lượng: m Q + m a x i t = m m u ố i + m N O + m H 2 O
hay 99,6 + 361,5a = 315,9 - 79,5a + 30.(7a - 3,85) +18.3,5a ⟺ a = 0,6
Vậy khối lượng muối trong dung dịch sau phản ứng là:
mmuối = 315,9 - 79,5.0,6 = 268,2 (gam)
Đáp án A.
hòa tan hết m gam hỗn hợp X gồm Fe,Cu và FeO (trong đó số mol Cu bằng số mol FeO) trong dung dịch HNO3, thu được a mol khí NO và dung dịch Y chứa hai muối. Thêm dung dịch HCl dư vào Y thu được b mol khí NO (NO là sản phẩm khử duy nhất). Tỉ lệ a:b là
Coi \(n_{Cu} = n_{FeO} = 1(mol)\\ n_{Fe} = x(mol)\)
Bảo toàn electron cho quá trình 1:
\(2n_{Fe} + 2n_{Cu} = 3n_{NO}\)
⇒ 2x + 2 = 3a(1)
Y gồm \(Cu(NO_3)_2,Fe(NO_3)_2\)
Bảo toàn electron cho quá trình 2 :
\(n_{Fe(NO_3)_2} = x + 1 = 3n_{NO}\)
⇒ x + 1 = 3b(2)
Lấy (1) : (2), ta có \(\dfrac{2x + 2}{x + 1} =\dfrac{3a}{3b} \Rightarrow \dfrac{a}{b} = 2\)
Hòa tan hết 19,76 gam hỗn hợp gồm Fe, FeO, Fe3O4, Fe2O3 trong dung dịch chứa 0,14 mol HNO3, 0,74 mol HCl, thu được 0,11 mol khí X và dung dịch Y (chỉ chứa muối trung hòa). Dung dịch Y hòa tan tối đa x gam bột Cu. Biết khí NO là sản phẩm khử duy nhất của cả quá trình và các phản ứng xảy ra hoàn toàn. Giá trị của x là.
A. 6,40
B. 5,12
C. 6,08
D. 6,72
Hòa tan hết 14,88 gam hỗn hợp X gồm Fe, FeO, Fe2O3 và Fe3O4 bằng dung dịch chứa 0,4 mol HCl và 0,41 mol HNO3, thu được dung dịch Y và 2,016 lít hỗn hợp khí Z gồm NO và NO2 tỷ lệ mol tương ứng 5:13 (đktc, không còn sản phẩm khử nào khác). Cho Cu (dư) vào dung dịch Y thì thầy có khí NO (duy nhất) thoát ra. Khối lượng Cu đã tham gia phản ứng là:
A. 7,68
B. 9,60
C. 9,28
D. 10,56
Hòa tan hết 21,56 gam hỗn hợp gồm Fe, FeO, Fe3O4, Fe2O3, Fe(OH)2 (trong đó Fe(OH)2 chiếm 8,35% khối lượng) trong dung dịch chứa 0,2 mol HNO3, 0,96 mol HCl, thu được 0,15 mol khí X và dung dịch Y. Cho Cu vào dung dịch Y thấy có m gam Cu phản ứng và thoát ra 0,448 lít khí X (đktc). Biết NO là sản phẩm khử duy nhất của cả quá trình, các phản ứng xảy ra hoàn toàn. Giá trị của m là.
A. 9,60
B. 10,24
C. 11,84
D. 6,72
Hòa tan hết 13,09 gam hỗn hợp X chứa Fe, Fe(OH)2 và Fe(OH)3 vào 0,85 lít dung dịch HNO3 1M thu được khí và dung dịch Y. Dung dịch Y hòa tan tối đa 11,2 gam Cu thu được khí và dung dịch Z. Biết NO là sản phẩm khử duy nhất của N+5. Tổng số mol khí thu được là?
A. 0,14 mol
B. 0,16 mol
C. 0,12 mol
D. 0,18 mol
Hòa tan hết 7,52 gam hỗn hợp X gồm Fe, FeO, Fe2O3 và Fe3O4 bằng dung dịch chứa 0,12 mol H2SO4 và 0,18 mol HNO3, thu được dung dịch Y và 0,896 lít hỗn hợp khí Z gồm NO và NO2 tỷ lệ mol tương ứng 1:3 (đktc, không còn sản phẩm khử nào khác). Cho Cu (dư) vào dung dịch Y thì thầy có a mol khí NO (duy nhất) thoát ra. Giá trị của a là:
A. 0,015
B. 0,02
C. 0,03
D. 0,01
Hòa tan hết 15,0g hỗn hợp X gồm Fe, Fe3O4, FeCO3 và Fe(NO3)2 trong dung dịch chứa NaHSO4 và 0,16 mol HNO3, thu được dung dịch Y và hỗn hợp khí Z gồm CO2 và NO (tỉ lệ mol 1: 4). Nếu cho dung dịch Y hòa tan tối đa 8,64g bột Cu, thấy thoát ra 0,03 mol NO. Nếu cho dung dịch Ba(OH)2 dư vào Y, thu được 154,4g kết tủa. Biết các phản ứng xảy ra hoàn toàn và khí NO là sản phẩm khử duy nhất của các quá trình. Phần trăm khối lượng của Fe đơn chất trong hỗn hợp X là:
A. 48,80
B. 33,60
C. 37,33
D. 29,87
Đáp án C
Có: nCu = 8,64: 64 = 0,135 mol ; nNO = 0,03 mol
nH+ dư = 4nNO = 4.0,03 = 0,12 mol (vì Cu + Y tạo khí NO => H+ dư ) => Y chỉ có Fe3+
- Khi Y + lượng Cu tồi đa => Fe3+ phản ứng hết (Cu + 2Fe3+ → Cu2+ + 2Fe2+)
Bảo toàn electron: nFe3+ + 3nNO = 2nCu => nFe3+ = 2.0,135 – 0,03.3 = 0,18 mol
Khi Y + Ba(OH)2 dư thì nFe(OH)3 = nFe3+ = 0,18 mol
mkết tủa = 154,4g = mFe(OH)3 + mBaSO4 => mBaSO4 = 154,4 – 107.0,18 = 135,14g
=> nBaSO4 = 0,58 mol
- Dung dịch Y chứa: Fe3+ (0,18 mol) ; SO42- (0,58 mol) ; Na+ (0,58 mol) ; H+ dư (0,12 mol)
Bảo toàn điện tích: 3nFe3+ + nNa+ + nH+ dư = 2nSO4 + nNO3 => nNO3 = 0,08 mol
Đặt a, b, c,d lần lượt là số mol của Fe, Fe3O4, FeCO3, Fe(NO3)2
=> mX = 56a + 232b + 116c + 180d = 15 (1)
-Bảo toàn nguyên tố Fe: nnguyên tố Fe(X) = a + 3b + c + d = 0,18 mol = nFe3+ (2)
- Bảo toàn C: nCO2 = nFeCO3 = c => Trong Z: nNO = 4c (vì nCO2: nNO = 1: 4)
X + hỗn hợp dung dịch thì:
Fe cho 3e ; Fe3O4 cho 1e (thực chất là FeO.Fe2O3 => FeO cho 1e) ; FeCO3 cho 1e ; Fe(NO3)2 cho 1e để tạo thành Fe3+
Bảo toàn electron: 3nFe + nFe3O4 + nFeCO3 + nFe(NO3)2 = 3nNO
=> 3a + b + c + d = 3.4c (3)
Bảo toàn N: 2nFe(NO3)2 + nHNO3 = nNO3 (Y) + 4nNO => 2d + 0,16 = 0,08 + 4c (4)
Giả hệ (1,2,3,4) => a = 0,1 ; b = 0,01 ; c = 0,03 ; d = 0,02 mol
=> %mFe = 0,1.56: 15 = 37,33%